Отметим, что устойчивость развивается не у человека, а у бактерий и других микроорганизмов.
«Резистентность может возникнуть естественным путем при постоянном контакте с антимикробными веществами. Многие антибиотики имеют природное происхождение, поэтому микроорганизмы нуждались в устойчивости к ним с тех пор, как на Земле существует жизнь, – рассказывает Лидия Доценко, руководитель службы отдела эпидемиологии инфекционных заболеваний Департамента здоровья. – Резистентность может появиться из-за случайных мутаций или передаваться между бактериями через обмен генетическим материалом, содержащим гены устойчивости. В результате естественного отбора выживают те микроорганизмы, которые способны переносить контакт с антимикробными веществами, тогда как те, кто не приобрёл устойчивость, погибают».
Как отмечает Янне Сепп, специалист Департамента лекарств, это означает, что бактерии учатся противостоять действию антибиотиков и становятся невосприимчивыми к лечению, формируя устойчивые к медикаментам штаммы.
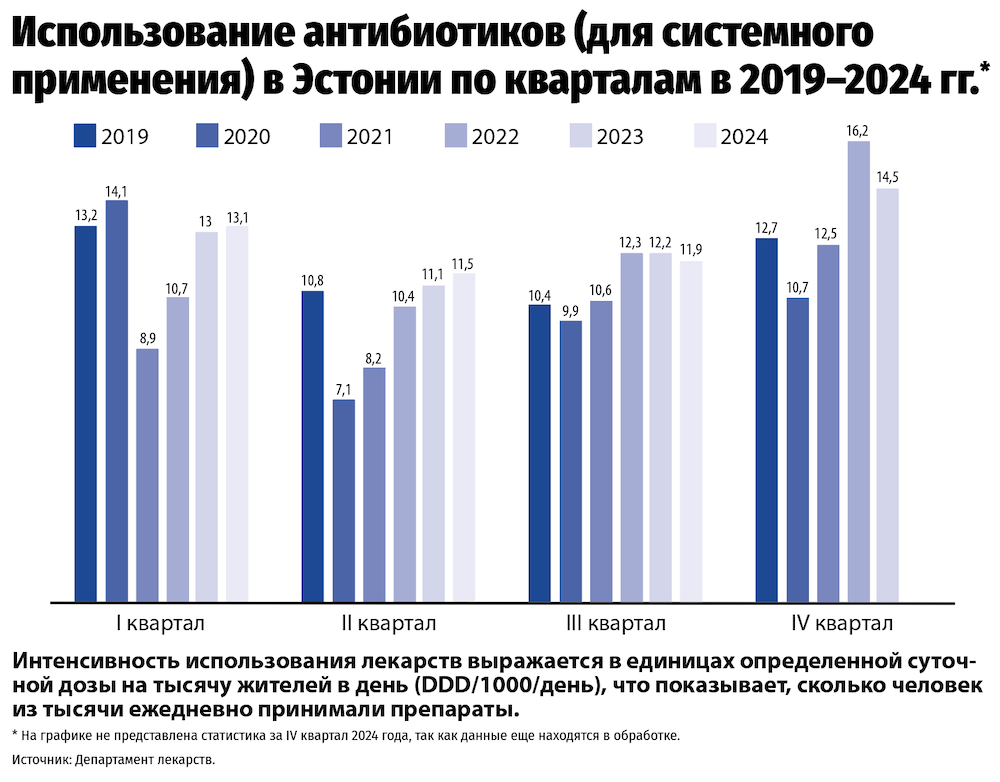
По ее словам, пандемия Covid‑19 и связанные с ней социальные ограничения оказали прямое влияние на распространение других инфекционных заболеваний, а также на потребление антибиотиков.
По всей Европе в этот период (2020–2021) использование антибиотиков значительно снизилось, в Эстонии – примерно на 11–14%. Если сравнивать постпандемийные годы (2022–2023) с допандемийным периодом (2019), можно отметить увеличение потребления антибиотиков примерно на 5–8% в год.
Вирус бактерии рознь
«Заболел ребенок, и мы подумали сначала, что это – вирус, который, как правило, проходит у него в течение недели, – рассказывает 30-летняя Наталья из Нарвы. – Через неделю сыну лучше не стало, добавился еще и кашель, и ему выписали антибиотики. Но и с ними не было заметного улучшения, поэтому мы поехали в ЭМО. Там сдали анализы, оказалось, что все-таки это был грипп, и антибиотики можно было не пить».
«Один из факторов, способствующих развитию устойчивости к антибиотикам, – их неправильное и чрезмерное применение», – говорит Янне Сепп.
Неправильное применение, например, – это когда антибиотиками начинают лечить вирусные инфекции.
«Согласно исследованиям, около 80% сезонных заболеваний носа, ушей, горла и легких вызывают вирусы, против которых антибиотики неэффективны. Их применение в этих случаях способствует развитию антибиотикорезистентности. Поэтому антибиотики следует использовать исключительно для лечения бактериальных инфекций», – подчеркивает специалист.
Другой немаловажный фактор – нарушение режима приема. Например, когда пациенты не соблюдают предписанную дозировку или преждевременно прекращают курс лечения.
Как поясняет Янне Сепп, если врач назначил антибиотики, крайне важно соблюдать схему лечения и всегда проходить курс до конца. Даже если самочувствие улучшилось уже через несколько дней, необходимо принимать лекарство ровно столько, сколько предписано, чтобы избежать выживания устойчивых к лечению бактерий и их дальнейшего размножения в организме.
Круговорот бактерий
Устойчивость к антимикробным препаратам – глобальная проблема, требующая комплексного подхода, отмечает Лидия Доценко.
По ее словам, для её решения необходимо международное сотрудничество и политические меры. В работе участвуют организации, такие как Всемирная организация здравоохранения (ВОЗ), Продовольственная и сельскохозяйственная организация ООН (ФАО) и Всемирная организация охраны здоровья животных (WOAH). Они продвигают концепцию «One Health» («Единое здоровье»), которая рассматривает проблему на уровне людей, животных и окружающей среды.
В Эстонии действует координационная группа при Министерстве социальных дел и разработана стратегия контроля за антибиотикорезистентностью.
«В разных странах мира доступность и практика применения антибиотиков сильно различаются. В Эстонии их можно получить только по рецепту, а в больницах тщательно контролируют их рациональное использование», – поясняет Янне Сепп.
Но не везде этот процесс регулируется.
«В некоторых странах антибиотики можно свободно купить в киосках, а также применять в качестве стимуляторов роста для животных – в ЕС такая практика была запрещена в 2006 году. Во многих странах антибиотики по-прежнему бесконтрольно и чрезмерно используют в животноводстве, что усугубляет проблему устойчивости к лекарствам», – говорит специалист.
Антибиотики так и или иначе попадают в окружающую нас среду. Подвергаемся ли мы опасности, если, например, купаемся в озере или море?
«Основная опасность нахождения антибиотиков в окружающей среде – это именно возникновение устойчивости у бактерий к лекарственным препаратам, – объясняет профессор Марина Кричевская, руководитель магистерской программы «Химическая технология и технологии защиты окружающей среды» в Институте технологий материалов и окружающей среды при Таллиннском техническом университете. – Проблема не в антибиотиках в окружающей среде, а в последствиях их присутствия – мутации микроорганизмов и угрозы попадания самих этих бактерий в организм человека или передачи ими мутированных генов бактериям, живущим в человеке».
То есть, как отмечает профессор Кричевская, потенциальная проблема – не собственно контакт человека с антибиотиками в окружающей среде, а контакт с бактериями, которые взаимодействовали с антибиотиками.
«Некоторые бактерии в окружающей среде и так нечувствительны к антибиотикам, но проблема возникает тогда, когда бактерии, которые были чувствительны, постепенно мутируют и развивают устойчивость, то есть резистентность, – подчеркивает Марина Кричевская. – И попадают антибиотики в окружающую среду из животноводства, через канализацию (после биологической очистки) в водоемы, с некачественной очисткой стоков фармацевтических производств».
Как отмечает профессор, рост резистентности связан, например, с повышением температуры окружающей среды и плотности населения – о чем свидетельствуют исследования в этой области.
Так, в американском исследовании, проведенном в 2018 году, было установлено, что увеличение температуры на 10 °C в различных регионах коррелирует с ростом устойчивости к антибиотикам на 4,2%, 2,2% и 2,7% у таких распространенных патогенов, как Escherichia coli, Klebsiella pneumoniae и Staphylococcus aureus соответственно.
Все эти бактерии могут стать причиной серьезных инфекций – от пневмонии и других заболеваний легких до остеомиелита, острых инфекций мочевого пузыря, печени, почек и т. п.
Например, устойчивые к антибиотикам штаммы mycobacterium tuberculosis (палочки Коха) угрожают свести на нет все достижения в борьбе с мировой эпидемией туберкулеза.
По данным ВОЗ, именно туберкулез – один из основных факторов, способствующих развитию антимикробной резистентности. Многорезистентный туберкулез – это форма данного заболевания, вызываемая бактериями, которые не реагируют на изониазид и рифампицин (два наиболее эффективных препарата от этой болезни).
Ученые не дремлют
ВОЗ констатирует: в 2021 году 1,14 миллиона смертей были напрямую связаны с антибиотикорезистентностью.
Лечение многих инфекционных болезней усложняется, зачастую требуются более дорогие и токсичные средства.
Вместе с тем, по данным ВОЗ, портфель клинических разработок новых противомикробных препаратов крайне мал. Нехватку препаратов испытывают страны всех уровней развития.
«Создание новых антибиотиков – сложный и длительный процесс, так как поиск новых механизмов действия требует глубоких молекулярно-биологических исследований, – поясняет Янне Сепп. – Большинство антибиотиков воздействуют на клеточную стенку бактерий, синтез белков или репликацию ДНК, однако нахождение новых «мишеней» (структур бактерий, на которые можно воздействовать) представляет значительные трудности. Кроме того, перед выходом на рынок новые препараты должны пройти строгие испытания на безопасность и эффективность, что делает процесс разработки дорогостоящим и долгосрочным».
По ее словам, для преодоления антибиотикорезистентности исследуют новые подходы. Один из них – использование вспомогательных молекул, которые усиливают действие антибиотиков.
«Например, так называемые ингибиторы бета-лактамаз предотвращают разрушение антибиотиков бактериями, позволяя препаратам эффективно выполнять свою функцию. Другой метод – применение иммуномодуляторов, которые укрепляют защитные силы организма против инфекций. Они помогают иммунной системе эффективнее реагировать на возбудителей, но не заменяют антибиотики, а лишь дополняют их действие», – отмечает специалист.
Пожиратели микробов
Альтернативой антибиотикам может стать фаговая терапия, которая в последние годы активно развивается. В Эстонии, по словам Янне Сепп, фаготерапия была впервые применена для лечения инфекции, устойчивой к антимикробным препаратам.
Бактериофаги, или фаги – это вирусы, поражающие только бактериальные клетки. Используемые с целью лечения фаги после заражения сначала размножаются в бактериальной клетке, а затем убивают ее. В результате высвобождаются новые фаги, которые, в свою очередь, заражают следующие бактерии. Фаги встречаются практически повсюду: как в окружающей среде, так и в организме человека.
Исследования, проведенные на сегодняшний день, показали, что фаготерапия – безопасный метод лечения и риск побочных эффектов низок.
Антибактериальный эффект бактериофагов был открыт более 100 лет назад, а в 1920–1930-е годы фаговая терапия была довольно популярной формой лечения. Однако интерес к фаготерапии угас в 1940-х годах – после открытия и внедрения пенициллина и других антибиотиков.
Для фаговой терапии используют бактерию пациента для поиска подходящего фага или их смеси из уже существующего банка фагов. Таким образом, в случае фаготерапии создают так называемый фаговый коктейль, подходящий пациенту. Такое персонализированное лекарство может быть эффективным, но его изготовление требует несколько иного подхода, чем тот, который используют в фармацевтической промышленности до сих пор.
В настоящее время в Европе не лицензированы никакие фаговые препараты для использования на людях. Фаг можно применять как готовый препарат и индивидуально для каждого пациента в ситуациях, когда больше ничего не помогает. В Эстонии для применения лекарств без регистрационного удостоверения требуется разрешение Департамента лекарств.
Что мы пьем?
Ежегодно в Балтийское море попадает 2200 тонн остатков лекарств, наносящих непоправимый урон морским организмам. Некоторые отходы не разлагаются, а значит – со временем могут оказаться и в питьевой воде.
«Что могут сделать международные организации – вести мониторинг использования антибиотиков и развития резистентности, снижать количества антибиотиков в сельском хозяйстве, использовать очистительные сооружения на производствах, – перечисляет профессор Кричевская. – А обычные люди – следовать рекомендациям врача при приеме лекарств и ни в коем случае не выбрасывать и не сливать в канализацию просроченные или неиспользованные лекарства. Можно бесплатно сдать на станциях по сбору отходов или отнести в аптеку до двух килограммов лекарственных отходов, которые образовались в домашнем хозяйстве».
Комментарий
Когда нужны антибактериальные препараты?
Андрей Борисов, семейный врач:
Антибиотики назначают не только тогда, когда болезнь запущена. Есть ряд заболеваний, при которых надо сразу начинать лечение антибиотиками – например, стрептококковая ангина, а есть заболевания, при которых не спешат с антибиотиками и дают возможность организму справиться самому.
При постановке диагноза исходят из симптомов, эпидемиологической ситуации, результатов осмотра и некоторых анализов.
Зачастую бактериальная инфекция бывает осложнением вирусной инфекции, поэтому тоже не сразу начинают давать антибиотик. Каждый случай – индивидуальный, поэтому надо контактировать с медицинским учреждением, где дадут конкретные и персональные рекомендации.
В любом случае, каждый человек должен уметь самостоятельно начать симптоматическое лечение, а дальше его будет корректировать врач, исходя из изменения симптоматики, находок при осмотре и результатов анализов.
Иногда антибиотик по ходу лечения меняют. Например, взяли посев и результат будет только через 4–5 дней, а человек с острым заболеванием не может ждать столько времени, вот тогда, и назначают антибиотик эмпирически. Но бывает, что после – в результатах посева (в антибиограмме) – врач видит, что данная бактерия устойчива к антибиотику, который человек уже принимает, и приходится менять препарат в соответствии с антибиограммой (которая показывает чувствительность бактерии к антибиотику). Это – обычная практика.
Обычно антибиотики дают быстрый эффект, где-то через три-четыре дня наступает облегчение, но все равно надо пропить курс лекарств до конца – даже если через три-четыре дня кажется, что уже все хорошо.
Три вопроса специалисту
Лидия Доценко, руководитель службы отдела эпидемиологии инфекционных заболеваний Департамента здоровья

– Почему распространяется антибиотикорезистентность (АБР)?
Несмотря на то, что АБР является естественным явлением, ее распространение ускоряется из-за чрезмерного и неправильного использования антибиотиков в медицине и животноводстве. Этому способствуют:
- Недостаточные санитарно-гигиенические условия, особенно плохая гигиена рук.
- Недостаточная профилактика инфекций с помощью вакцинации.
- Увеличение миграции людей, что способствует быстрому распространению инфекций.
- Загрязнение окружающей среды антибиотиками.
Резистентность может развиваться за недели, годы или десятилетия. Например, у бактерий Escherichia coli и Staphylococcus aureus резистентность может появляться уже через несколько недель или месяцев после начала применения антибиотика. В то же время у Streptococcus pneumoniae устойчивость к пенициллину формировалась десятилетиями.
– Можно ли измерить антибиотикорезистентность?
– Для оценки устойчивости бактерий используются методы микробиологического анализа. Патоген выделяется из клинического материала, после чего проводится тест на чувствительность к антибиотикам. Бактерии помещаются в среду с различными антибиотиками, и, если их рост останавливается, значит, они чувствительны к этому препарату. Если рост продолжается, бактерии устойчивы, и данный антибиотик будет неэффективен.
Семейный врач может назначить такой анализ при подозрении на бактериальную инфекцию или если стандартное лечение антибиотиками не дало результата.
– Как отличить вирусную инфекцию от бактериальной, чтобы не запоздать с лечением?
– Сложно, симптомы могут совпадать. Врач может провести клиническую оценку или назначить лабораторные тесты.
При вирусных инфекциях антибиотики не помогают. Лечение направлено на облегчение симптомов.
Антибиотики назначаются только при бактериальных инфекциях, но не во всех случаях. Для выбора правильного антибиотика может потребоваться микробиологический анализ или врачебное решение на основе типа инфекции.
Обратиться к врачу следует, если после улучшения симптомы снова ухудшаются, возникает высокая температура или резко ухудшается самочувствие.
Памятка для пациента
- Антибиотики действуют только против бактериальных инфекций. При вирусных заболеваниях, таких как грипп и другие простудные болезни, антибиотики бесполезны.
- Принимайте антибиотики строго по назначению врача и не прекращайте курс раньше положенного срока, даже если вам стало лучше, иначе выжившие бактерии могут стать устойчивыми.
- Не принимайте антибиотики самостоятельно и не делитесь ими с другими – каждое заболевание требует подходящего лечения, и неправильное применение антибиотиков может принести больше вреда, чем пользы.
- Не выбрасывайте неиспользованные антибиотики в бытовой мусор или канализацию – попадая в окружающую среду, они способствуют развитию устойчивых бактерий. Остатки лекарств следует сдавать в пункт сбора опасных отходов, на станцию утилизации или в аптеку.